Muallif:
Mark Sanchez
Yaratilish Sanasi:
3 Yanvar 2021
Yangilanish Sanasi:
1 Iyul 2024

Tarkib
- Qadamlar
- 2 -usul 1: Belgilangan og'irliklarga asoslangan massa foizini aniqlash
- 2 -usul 2: Hech qanday massa aniqlanmaganida massa foizini aniqlash
Massa ulushi kimyoviy birikmadagi elementlarning foizini ko'rsatadi. Massa foizini topish uchun siz birikmaga kiritilgan elementlarning molyar massasini (mol boshiga grammda) yoki ma'lum bir eritmani olish uchun har bir komponentning gramm sonini bilishingiz kerak.Massa ulushi juda oddiy hisoblanadi: elementning (yoki komponentning) massasini butun aralashmaning (yoki eritmaning) massasiga bo'lish kifoya.
Qadamlar
2 -usul 1: Belgilangan og'irliklarga asoslangan massa foizini aniqlash
 1 Kimyoviy birikmaning og'irlik foizini aniqlash uchun tenglamani tanlang. Massa ulushi quyidagi formula yordamida hisoblanadi: massa foizi = (komponent massasi / birikmaning umumiy massasi) x 100. Foiz olish uchun bo'linish natijasi 100 ga ko'paytiriladi.
1 Kimyoviy birikmaning og'irlik foizini aniqlash uchun tenglamani tanlang. Massa ulushi quyidagi formula yordamida hisoblanadi: massa foizi = (komponent massasi / birikmaning umumiy massasi) x 100. Foiz olish uchun bo'linish natijasi 100 ga ko'paytiriladi. - Muammoni hal qilishning boshida tenglikni yozing: massa foizi = (komponent massasi / birikmaning umumiy massasi) x 100.
- Sizni qiziqtirgan komponentning massasi muammoning holatida bo'lishi kerak. Agar massa berilmasa, noma'lum massa bilan massa foizini qanday aniqlash mumkinligi haqidagi keyingi bo'limga o'ting.
- Kimyoviy birikmaning umumiy massasi bu birikmaning (yoki eritmaning) bir qismi bo'lgan barcha elementlarning (komponentlarning) massalarini qo'shish orqali topiladi.
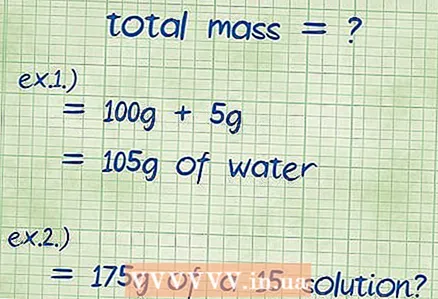 2 Murakkabning umumiy massasini hisoblang. Agar siz birikmani tashkil etuvchi barcha komponentlarning massasini bilsangiz, ularni qo'shib qo'ying va shu tarzda hosil bo'lgan birikma yoki eritmaning umumiy massasini topasiz. Siz bu massani massa foiziga tenglamangizda maxraj sifatida ishlatasiz.
2 Murakkabning umumiy massasini hisoblang. Agar siz birikmani tashkil etuvchi barcha komponentlarning massasini bilsangiz, ularni qo'shib qo'ying va shu tarzda hosil bo'lgan birikma yoki eritmaning umumiy massasini topasiz. Siz bu massani massa foiziga tenglamangizda maxraj sifatida ishlatasiz. - Misol 1: 100 gramm suvda erigan 5 gramm natriy gidroksidning massa ulushi qancha?
- Eritmaning umumiy massasi natriy gidroksidi va suv miqdori yig'indisiga teng: 100 g + 5 g 105 g beradi.
- 2 -misol: 175 gramm 15 foizli eritmani tayyorlash uchun qancha natriy xlor va suv kerak?
- Bu misolda umumiy massa va kerakli foiz berilgan va eritmaga qo'shilishi kerak bo'lgan moddaning miqdorini topish talab qilinadi. Umumiy vazni 175 gramm.
- Misol 1: 100 gramm suvda erigan 5 gramm natriy gidroksidning massa ulushi qancha?
 3 Belgilangan komponentning massasini aniqlang. Agar sizdan "massa foizi" ni hisoblash so'ralsa, ma'lum bir komponentning massasi necha foizni tashkil etishi aniqlanishi kerak. Belgilangan komponentning massasini yozib oling. Bu massa ulushi uchun formulada hisoblagich bo'ladi.
3 Belgilangan komponentning massasini aniqlang. Agar sizdan "massa foizi" ni hisoblash so'ralsa, ma'lum bir komponentning massasi necha foizni tashkil etishi aniqlanishi kerak. Belgilangan komponentning massasini yozib oling. Bu massa ulushi uchun formulada hisoblagich bo'ladi. - 1 -misol: Berilgan komponentning massasi - natriy gidroxlorid - 5 gramm.
- 2 -misol: Bu misolda berilgan komponentaning massasi noma'lum va uni topish kerak.
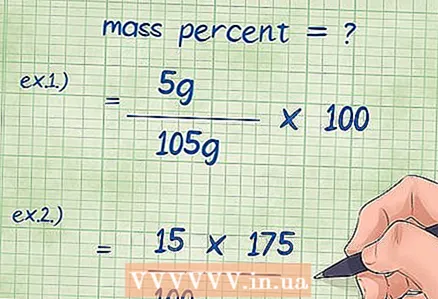 4 Qiymatlarni massa foiz tenglamasiga ulang. Barcha kerakli qiymatlarni aniqlagandan so'ng, ularni formulaga ulang.
4 Qiymatlarni massa foiz tenglamasiga ulang. Barcha kerakli qiymatlarni aniqlagandan so'ng, ularni formulaga ulang. - 1 -misol: massa foizi = (komponent massasi / birikmaning umumiy massasi) x 100 = (5 g / 105 g) x 100.
- 2 -misol: kimyoviy komponentning noma'lum massasini topish uchun massa foiz formulasini o'zgartirish kerak: komponent massasi = (massa ulushi * birikmaning umumiy massasi) / 100 = (15 * 175) / 100.
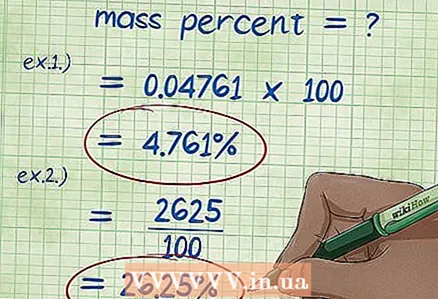 5 Massa foizini hisoblang. Formuladagi barcha qiymatlarni massa foiziga almashtirgandan so'ng, kerakli hisoblarni bajaring. Komponentning massasini kimyoviy birikma yoki eritmaning umumiy og'irligiga bo'linib 100 ga ko'paytiring. Natijada bu komponentning massa foizi olinadi.
5 Massa foizini hisoblang. Formuladagi barcha qiymatlarni massa foiziga almashtirgandan so'ng, kerakli hisoblarni bajaring. Komponentning massasini kimyoviy birikma yoki eritmaning umumiy og'irligiga bo'linib 100 ga ko'paytiring. Natijada bu komponentning massa foizi olinadi. - 1 -misol: (5/105) x 100 = 0,04761 x 100 = 4,761%. Shunday qilib, 100 gramm suvda erigan 5 gramm natriy gidroxloridning og'irlik ulushi 4,761%ni tashkil qiladi.
- 2 -misol: Komponentning massa ulushi uchun qayta yozilgan ifoda (massa ulushi * moddaning umumiy massasi) / 100, shundan biz topamiz: (15 * 175) / 100 = (2625) / 100 = 26,25 gramm natriy xlorid.
- Eritmaning umumiy massasidan komponentning massasini chiqarib, kerakli miqdordagi suvni topamiz: 175 - 26,25 = 148,75 gramm suv.
2 -usul 2: Hech qanday massa aniqlanmaganida massa foizini aniqlash
 1 Kimyoviy birikmaning og'irlik foizi uchun formulani tanlang. Massa foizini topishning asosiy tenglamasi quyidagicha: massa foiz = (elementning molyar massasi / birikmaning umumiy molekulyar massasi) x 100. Moddaning molyar massasi - bu ma'lum bir moddaning bir molining massasi, molekulyar massasi bu butun kimyoviy birikmalarning bir molining massasi. Foizlarni olish uchun bo'linma 100 ga ko'paytiriladi.
1 Kimyoviy birikmaning og'irlik foizi uchun formulani tanlang. Massa foizini topishning asosiy tenglamasi quyidagicha: massa foiz = (elementning molyar massasi / birikmaning umumiy molekulyar massasi) x 100. Moddaning molyar massasi - bu ma'lum bir moddaning bir molining massasi, molekulyar massasi bu butun kimyoviy birikmalarning bir molining massasi. Foizlarni olish uchun bo'linma 100 ga ko'paytiriladi. - Muammoni hal qilishning boshida tenglikni yozing: massa foiz = (elementning molyar massasi / birikmaning umumiy molekulyar massasi) x 100.
- Ikkala miqdor ham mol boshiga gramm bilan o'lchanadi (g / mol).
- Agar sizga massalar berilmasa, ma'lum bir moddaning elementning massa ulushini molyar massa yordamida topish mumkin.
- Misol 1: Suv molekulasidagi vodorodning massa ulushini toping.
- 2 -misol: Glyukoza molekulasidagi uglerodning massa ulushini toping.
 2 Kimyoviy formulani yozing. Agar misolda ko'rsatilgan moddalarning kimyoviy formulalari berilmagan bo'lsa, ularni o'zingiz yozib olishingiz kerak. Agar vazifada kimyoviy moddalar uchun kerakli formulalar bo'lsa, siz bu bosqichni o'tkazib yuborib, to'g'ridan -to'g'ri keyingi bosqichga o'tishingiz mumkin (har bir elementning massasini toping).
2 Kimyoviy formulani yozing. Agar misolda ko'rsatilgan moddalarning kimyoviy formulalari berilmagan bo'lsa, ularni o'zingiz yozib olishingiz kerak. Agar vazifada kimyoviy moddalar uchun kerakli formulalar bo'lsa, siz bu bosqichni o'tkazib yuborib, to'g'ridan -to'g'ri keyingi bosqichga o'tishingiz mumkin (har bir elementning massasini toping). - 1 -misol: Suvning kimyoviy formulasini yozing, H2O.
- 2 -misol: glyukozaning kimyoviy formulasini yozing, C6H12O6.
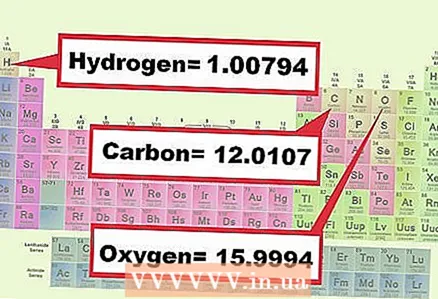 3 Murakkab tarkibidagi har bir elementning massasini toping. Kimyoviy formuladagi har bir elementning molyar og'irligini davriy jadval bo'yicha aniqlang. Odatda, elementning massasi uning kimyoviy belgisi ostida ko'rsatiladi. Tegishli birikmani tashkil etuvchi barcha elementlarning molyar massalarini yozing.
3 Murakkab tarkibidagi har bir elementning massasini toping. Kimyoviy formuladagi har bir elementning molyar og'irligini davriy jadval bo'yicha aniqlang. Odatda, elementning massasi uning kimyoviy belgisi ostida ko'rsatiladi. Tegishli birikmani tashkil etuvchi barcha elementlarning molyar massalarini yozing. - 1 -misol: Kislorod (15.9994) va vodorod (1.0079) ning molyar massalarini toping.
- 2 -misol: Uglerod (12.0107), kislorod (15.9994) va vodorod (1.0079) ning molyar massalarini toping.
 4 Har bir elementning molyar massasini uning molyar fraktsiyasiga ko'paytiring. Berilgan kimyoviy tarkibda har bir elementning nechta molini, ya'ni elementlarning mol ulushlarini aniqlang. Mol kasrlari formuladagi element belgilarining pastki qismidagi raqamlar bilan beriladi. Har bir elementning molyar massasini uning molyar qismiga ko'paytiring.
4 Har bir elementning molyar massasini uning molyar fraktsiyasiga ko'paytiring. Berilgan kimyoviy tarkibda har bir elementning nechta molini, ya'ni elementlarning mol ulushlarini aniqlang. Mol kasrlari formuladagi element belgilarining pastki qismidagi raqamlar bilan beriladi. Har bir elementning molyar massasini uning molyar qismiga ko'paytiring. - 1 -misol: vodorod belgisi ostida 2 ta, kislorod belgisi ostida 1 ta (raqam yo'qligiga teng). Shunday qilib, vodorodning molyar massasini 2 ga ko'paytirish kerak: 1.00794 X 2 = 2.01588; biz kislorodning molyar massasini bir xilda qoldiramiz, 15.9994 (ya'ni 1 ga ko'paytiramiz).
- 2 -misol: uglerod belgisi ostida 6, vodorod ostida 12 va kislorod ostida 6, elementlarning molyar massalarini shu sonlarga ko'paytirib, biz quyidagilarni topamiz:
- uglerod: (12.0107 * 6) = 72.0642
- vodorod: (1.00794 * 12) = 12.09528
- kislorod: (15.9994 * 6) = 95.9964
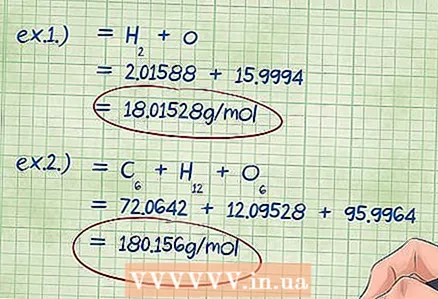 5 Murakkabning umumiy massasini hisoblang. Bu birikma tarkibiga kirgan barcha elementlarning topilgan massalarini qo'shing. Elementlarning mol massalarining mol fraktsiyalariga ko'payishi sizga kimyoviy birikmaning umumiy massasini beradi. Bu raqam massadagi foizlar uchun formulada bo'luvchi hisoblanadi.
5 Murakkabning umumiy massasini hisoblang. Bu birikma tarkibiga kirgan barcha elementlarning topilgan massalarini qo'shing. Elementlarning mol massalarining mol fraktsiyalariga ko'payishi sizga kimyoviy birikmaning umumiy massasini beradi. Bu raqam massadagi foizlar uchun formulada bo'luvchi hisoblanadi. - 1 -misol: 2.01588 g / mol (ikki mol vodorod atomining massasi) 15.9994 g / mol (bir mol kislorod atomining massasi) ga qo'shing, natijada 18.01528 g / mol bo'ladi.
- 2 -misol: Topilgan molyar massalarni qo'shing: uglerod + vodorod + kislorod = 72.0642 + 12.09528 + 95.9964 = 180.156 g / mol.
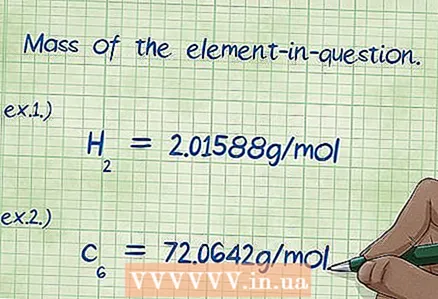 6 Qiziqarli elementning massasini aniqlang. Agar sizdan "massa ulushi" ni topishingiz so'ralsa, unda siz birikmaning bir qismi bo'lgan ma'lum bir elementning massasini barcha elementlarning umumiy massasining foiziga hisoblashingiz kerak. Berilgan elementning massasini toping va yozing. Buning uchun elementning molyar massasini uning molyar ulushiga ko'paytirish kerak. Natijada siz massa ulushi uchun formulaning hisoblagichidagi qiymatni olasiz.
6 Qiziqarli elementning massasini aniqlang. Agar sizdan "massa ulushi" ni topishingiz so'ralsa, unda siz birikmaning bir qismi bo'lgan ma'lum bir elementning massasini barcha elementlarning umumiy massasining foiziga hisoblashingiz kerak. Berilgan elementning massasini toping va yozing. Buning uchun elementning molyar massasini uning molyar ulushiga ko'paytirish kerak. Natijada siz massa ulushi uchun formulaning hisoblagichidagi qiymatni olasiz. - 1 -misol: Murakkab tarkibidagi vodorod massasi 2,01588 g / mol (ikki mol vodorod atomining massasi).
- 2 -misol: Murakkab tarkibidagi uglerod massasi 72,0642 g / mol (olti mol uglerod atomining massasi).
 7 Sonli qiymatlarni massa foiz tenglamasiga almashtiring. Barcha miqdorlarning qiymatlarini aniqlagandan so'ng, ularni birinchi bosqichda berilgan formulaga ulang: massa foizi = (elementning molyar massasi / birikmaning umumiy molekulyar massasi) x 100.
7 Sonli qiymatlarni massa foiz tenglamasiga almashtiring. Barcha miqdorlarning qiymatlarini aniqlagandan so'ng, ularni birinchi bosqichda berilgan formulaga ulang: massa foizi = (elementning molyar massasi / birikmaning umumiy molekulyar massasi) x 100. - 1 -misol: massa foizi = (elementning molyar massasi / birikmaning umumiy molekulyar massasi) x 100 = (2.01588 / 18.01528) x 100.
- 2 -misol: massa foizi = (elementning molyar massasi / birikmaning umumiy molekulyar massasi) x 100 = (72.0642 / 180.156) x 100.
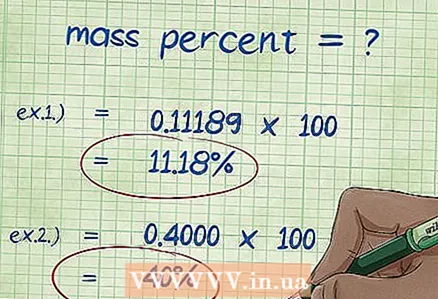 8 Massa foizini hisoblang. Sonli qiymatlarni almashtirgandan so'ng, kerakli arifmetik amallarni bajaring.Element massasini birikmaning umumiy massasiga bo'linib, 100 ga ko'paytiring. Natijada elementning massa ulushi olinadi.
8 Massa foizini hisoblang. Sonli qiymatlarni almashtirgandan so'ng, kerakli arifmetik amallarni bajaring.Element massasini birikmaning umumiy massasiga bo'linib, 100 ga ko'paytiring. Natijada elementning massa ulushi olinadi. - 1 -misol: massa foizi = (elementning molyar massasi / birikmaning umumiy molekulyar massasi) x 100 = (2.01588 / 18.01528) x 100 = 0.111189 x 100 = 11.18%. Shunday qilib, suv molekulasidagi vodorod atomlarining massa ulushi 11,18%ni tashkil qiladi.
- 2 -misol: massa foizi = (elementning molyar massasi / birikmaning umumiy molekulyar massasi) x 100 = (72.0642 / 180.156) x 100 = 0.4000 x 100 = 40.00%. Shunday qilib, glyukoza molekulasidagi uglerod atomlarining og'irlik ulushi 40,00%ni tashkil qiladi.



